Giải bài tập hóa lớp 10
Giải bài tập trang 13, 14 bài xích 2: hạt nhân nguyên tử - Nguyên tố hóa học - Đồng vị Sách giáo khoa (SGK) hóa học 10. Câu 1: thành phần hoá học là các nguyên tử gồm cùng...
Bạn đang xem: Giải bài tập hóa lớp 10
Bài 1 trang 13 sgk hoá học tập 10
Nguyên tố hoá học tập là số đông nguyên tử bao gồm cùng
A. Số khối. C. Sô" proton.
B. Số nơtron. D. Số nơtron và số proton.
Chọn C.
Bài 2 trang 13 sgk hoá học tập 10
Kí hiệu nguyên tử thể hiện đầy đủ đặc thù cho một nguyên tử của một thành phần hoá học vị nó cho biết
A. Số khối A. C. Nguyên tử khối của nguyên tử.
B. số hiệu nguyên tử z. D. Số khối A với số hiệu nguyên tử z.
Chọn đáp án đúng.
Lời giải:
Chọn D
Bài 3 trang 14 sgk hoá học 10
Nguyên tố cacbon tất cả hai đồng vị :
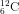
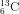
Nguyên tử khối mức độ vừa phải của cacbon là :
a) 12,500; b) 12,011 c) 12,022; d) 12,055.
Lời giải:
Chọn B.
Xem thêm: Đĩa Xoay Eo Tập Thể Dục - Đĩa Xoay Eo Có Tác Dụng Gì
Bài 4 trang 14 sgk hoá học 10
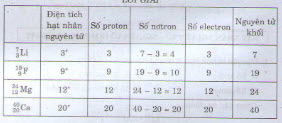
Hãy xác định diện tích phân tử nhân, số proton, số nơtron, số electron, nguyên tử khối của các nguyên tử thuộc các nhân tố sau:
( _3^7 extrmLi); ( _9^19 extrmF); ( _12^24 extrmMg); ( _20^40 extrmCa).
Lời giải:
Bài 5 trang 14 sgk hoá học tập 10
Đồng tất cả hai đồng vị ( _29^65 extrmCu) và ( _29^63 extrmCu). Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần xác suất của từng đồng vị.
Lời giải:
Gọi x là yếu tắc % của đồng vị 65Cu. Ta gồm :
( frac65x+63(100-x)100) = 63,54
Giải ra ta được X = 27% 65Cu. Vậy nhân tố 63Cu là 73%.
Bài 6 trang 14 sgk hoá học tập 10
Hiđro tất cả nguyên tử khối là 1,008. Hỏi gồm bao nhiêu nguyên tử của đồng vị ( _1^2 extrmH)trong 1ml nước (cho rằng nội địa chỉ tất cả đồng vị ( _1^2 extrmH) và ( _1^1 extrmH))? (Cho trọng lượng riêng của nước là một trong g/ml).
Lời giải:
Gọi % đồng vị ( _1^2 extrmH) là a:
( frac1(100-a)+2a100) = 1,008 => a = 0,8; %( _1^2 extrmH) là 0,8%
m của 1ml H2O: 1 gam
( M_H_2O) = 16 + 2,016 = 18,016u
—> khối lượng của 1 mol H20 là 18,016g.
Số nguyên tử H bao gồm trong 1ml H20
( frac1.6.10^23.218,016) = 0,666.1023 nguyên tử = 666.1020 nguyên tử
18,016
Số nguyên tử ( _1^2 extrmH) chiếm: ( frac666.10^20.0,8100) = 5,325.1020 nguyên tử.
Bài 7 trang 14 sgk hoá học 10
Oxi thoải mái và tự nhiên là một láo hợp các đồng vị: 99,757% 16O; 0,039% 17O; 0,204% 18O. Tính số nguyên tử của mỗi một số loại đồng vị khi có 1 nguyên tử 17O.
Lời giải:
Tỉ lệ mỗi đồng vị O trong các thành phần hỗn hợp 3 đồng vị:
99,757% 16O => 99757 nguyên tử 16O
0,039% 17O => 39 nguyên tử 17O
0,204% 18O => 204 nguyên tử 18O
Khi tất cả một nguyên tử 17O thì số nguyên tử:
16O là: (99757 over 39) = 2558 nguyên tử.
18O là: (204 over 29) = 5 nguyên tử.
Bài 8 trang 14 sgk hoá học tập 10
Agon tách ra từ bầu không khí là hỗn hợp bố đồng vị : 99,6% 40Ar; 0,063% 38Ar; 0,337% 36Ar. Tính thể tích của 10g Ar ở điều kiện tiêu chuẩn.









